主诉:
53 岁,男性。间断腹胀 2 年,加重伴眼黄、皮肤黄 2 周。
现病史:
2 年前患者因腹胀、乏力就诊,发现 HBsAg(+)、HBeAg(-)、HBV DNA 2.46×105 IU/mL,上腹部影 CT 示肝硬化,大量腹水,院内给予降门脉压、利尿、输白蛋白及抗感染治疗和恩替卡韦抗病毒治疗。病情稳定后出院门诊随访。
1 年前住院复查,肝功能稳定,HBV DNA< 检测下限,腹水消退,继续恩替卡韦治疗。
半年前患者自行停用恩替卡韦。
2 周前患者出现腹胀、乏力、炎黄、尿黄,门诊查肝功能 TBIL 203 µmol/L、DBIL 159 µmol/L、ALB 34.4 g/L、 ALT 995 U/L、AST 429 U/L,2019 年 1 月 28 日收住入院。
个人史:
吸烟 30 年,3-5 支/日,未戒烟。
饮酒 30 年,3-4 次/周,500 g 白酒/次,戒酒 2 年。
家族史:
否认乙肝家族史
院内查体:
慢性肝病面容,神志清楚。全身皮肤未见出血点,肝掌阳新,未见蜘蛛痣。全身皮肤重度黄染,巩膜重度黄染。心肺(-),腹平软,无压痛、反跳痛,肝脏肋下未触及,脾脏肋下 3 cm,质韧,无压痛,移动性浊音阴性,肠鸣音正常。脊柱四肢(-)。双下肢无水肿。踝阵挛(-),扑翼样震颤(-)。
实验室检查:
血常规:HB 146 g/L、 WBC 5.22×109/L、 NEUT% 78.6% 、PLT 38×109/L
肝肾功:TBIL 601 µmol/L↑、 DBIL 525 µmol/L↑、 IDBIL 76 µmol/L↑、 ALB 28.9 g/L↑ 、ALT 110 U/L↑、 AST 197 U/L↑ 、ALP 176 U/L↑、 GGT 70 U/L↑、CR 59 µmol/L
凝血:PT 19.3s↑ 、INR 1.65↓
AFP:239 ng/mL↑
高敏 HBV DNA:7.10×102IU/mL↑
乙肝标志物:HBsAg 93IU/mL↑
PCT:0.48ng/mL
CRP:17 mg/L
CT 检查:
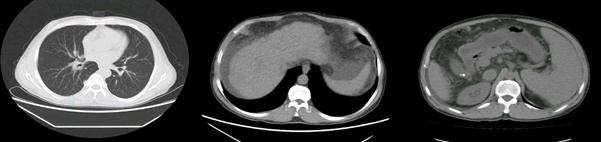
入院诊断:
慢加急性肝衰竭 C 型(MELD 评分 25 分)
病毒性肝炎 乙型 肝炎肝硬化失代偿期(Child-Pugh C 级 10 分)
腹水形成
治疗过程:
1. 抗乙肝病毒:丙酚替诺福韦酯
2. 维持内环境稳定与平衡
3. 补充热量、维生素,输注血浆、白蛋白
4. 肠道管理、人工肝支持
6. 监测感染相关症状、体征及实验室检查
治疗期间相关指标变化:
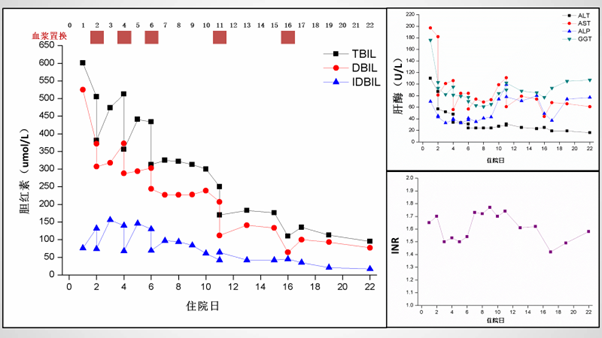
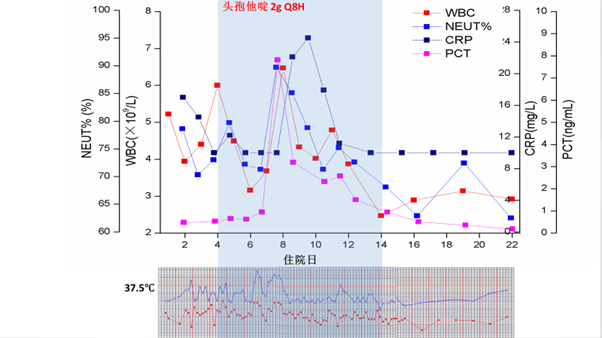
治疗 22 天后患者出院,出院时患者情况:
血常规:HB 111 g/L、WBC 2.29×109/L、NEUT% 62.5% 、PLT 32×109/L
肝肾功:TBIL 95 µmol/L↑、 DBIL 77 µmol/L↑、 IDBIL 17 µmol/L、 ALB 37.7 g/L、 ALT 16U/L、AST 61U/L↑、 ALP 107 U/L、GGT 77 U/L↑、 CR 46 µmol/L
凝血:PT 18.6s ↑ 、INR 1.58↓
AFP:29 ng/mL
高敏 HBV DNA:4.64×101IU/mL(较前下降>1 log)
乙肝标志物:HBsAg 161 IU/mL↑
PCT:0.18ng/mL
CRP:<10 mg/L
病例分析:
该病例是一位乙型肝炎相关慢加急肝衰竭(CHB-ACLF)患者,入院后积极进行综合治疗和使用丙酚替诺福韦酯(TAF)抗病毒治疗后获得良好效果。
慢加急性肝衰竭(ACLF)是临床上非常常见的一个综合征,起病急、死亡率高,因此在临床处理上有很多挑战。与欧美地区不同,亚洲 80% 以上 ACLF 与 HBV 感染密切相关 [1]。大量 HBV 活跃复制是 HBV-ACLF 发病的本质,虽然多数情况下 HBV 肝炎活动是自发性的,但 NA 治疗中不规范停药、NA 治疗耐药也是肝炎活动爆发的常见原因 [2]。患者并发 ACLF 时,HBV 大量繁衍复制,形成乙肝核心抗体等免疫反应,导致肝细胞短期内大量坏死,可进一步发展为肝功能衰竭和(或)肝外脏器功能衰竭,甚至发展为多脏器功能衰竭危及生命 [2-3]。此类患者若得不到及时有效的治疗,短期死亡率很高 [2-3]。因此,尽早抗病毒治疗,抑制机体内肝细胞病毒的复制有助于缓解患者过强的免疫反应,减少大面积肝细胞坏死情况,对改善 HBV 感染所致慢加急性肝衰竭患者预后至关重要。
研究表明,NAs 抗病毒治疗可以提高早期 HBV-ACLF 的生存率 [4-5],并且发现早期快速降低 HBV DNA 水平与患者更好的预后密切相关 [5]。提示患者可能获益于具有强效抗病毒效果的 NAs。指南也强调 HBV 引起的肝炎活动、失代偿、肝衰竭患者应立即使用快速强效的 NAs 抗病毒治疗 [6-8]。
TAF、TDF、ETV 是目前指南推荐的强效低耐药 NAs[8]。荟萃分析表明,ETV 治疗 HBV-ACLF 的长期生存率优于 LAM[9]。但需要注意 ETV 治疗 ACLF 存在乳酸酸中毒不良反应。文献报道,ETV 用于 16 例失代偿期肝硬化患者,5 例出现严重乳酸酸中毒,其中 1 例死亡 [10]。并且有研究显示,HBV-ACLF 患者使用 TDF 治疗的短期抗病毒疗效和长期预后均优于 ETV[11]。该前瞻性研究中纳入 67 例 HBV-ACLF 患者,分别给予 TDF 300 mg/d 或 ETV 0.5 mg/d 治疗,随访 3 个月,评估患者的生存率。结果显示,在治疗第 2 周时,TDF 组的 HBV DNA 下降水平显著优于 ETV 组(2.08 log10 IU/mL vs. 1.61 log10 IU/mL,P = 0.001),并且能使更多患者在 2 周内达到 HBV DNA 完全病毒学应答率(18.8% vs 0%,P = 0.007)。治疗 2 周内 TDF 组的 Child-Turcotte-Pugh(CTP)分级和终末期肝病模型(MELD)评分改善也显著优于 ETV 组(P<0.01)。至治疗 3 个月,TDF 组和 ETV 组分别有 34.4% 和 65.7% 的患者死亡,因此,TDF 治疗 3 个月的累计生存率也显著高于 ETV(65% vs 31.1%,P = 0.025)(图 1)。

图 1 TDF 和 ETV 治疗 HBV-ACLF 的生存率
由于 HBV-ACLF 常伴有肝外器官受累,肾脏是主要的受累器官之一,文献报道 TDF 会导致肾损伤,因此对于这类患者,骨肾安全性更优的 TAF 是更好的选择。TAF 的全球 III 期临床研究 [12],25 mg 的 TAF 抑制 HBV 复制的作用与 300 mg TDF 相当,但对肾脏功能的影响更小,eGFRCG 的下降更少(图 2),近端小管蛋白尿标志物的变化更小。对于轻、中、重度肾功能不全患者使用 TAF 无需调整剂量 [13]。
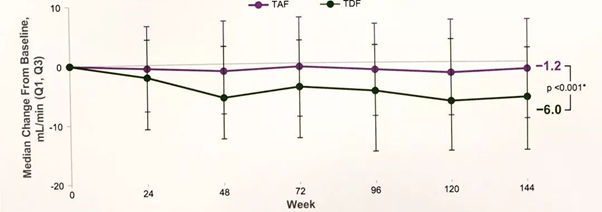
图 2. TAF 对比 TDF III 期研究 144 周的 eGFR 变化
除具有更优的肾脏和骨骼安全性外,TAF 的整体安全性和耐受性有所提升,绝大部分不良事件为轻~中度 [13]。因应用 TDF 时曾有过乳酸性酸中毒和伴脂肪变性的严重肝肿大病例报道 [14],TAF 上市之初 FDA 也就这两种情况在 TAF 标签中做出了黑框警告。TAF 上市不到半年,2017 年 4 月,美国 FDA 同意取消了这部分黑框警告的内容 [15],目前在中国已经获批的 TAF 说明书中,没有黑框警告。这也是 TAF 安全性提升的体现。
参考文献:
1. Satin SK, Kedarisetty CK, Abbas z, et a1. Acute-on-chronic liver failure: consensus recommendations of the Asian Pacific Association for the Study of the Liver(APASL) 2014. Hepatol Int, 2014, 8: 453-471.
2. Zhao RH, Shi Y, Zhao H, et al. Acute-on-chronic liver failure in chronic hepatitis B: an update. Expert Rev Gastroenterol Hepatol. 2018 Apr;12(4):341-350.
3. 戴金津, 朱传武, 蔡伟, 等. 恩替卡韦早期抗病毒治疗对乙型肝炎相关慢加急性肝衰竭转归的影响. 肝脏. 2018, 23(10): 873-877.
4. 刘慧敏, 毛青, 等. 核苷 (酸) 类似物抗病毒治疗对早期乙型肝炎病毒相关性慢加急性肝衰竭患者预后的影响. 第三军医大学学报, 2017, 39(24): 2412-2417.
5. Garg H, Sarin SK, Kumar M, et al. Tenofovir improves the outcome in patients with spontaneous reactivation of hepatitis B presenting as acute-on-chronic liver failure. Hepatology. 2011; 53: 774–780.
6. 中华医学会肝病学分会, 中华医学会感染病学分会. 慢性乙型肝炎防治指南(2015 年版). 中国肝脏病杂志(电子版),2015, 7(3): 1-18.
7. 中华医学会感染病学分会肝衰竭与人工肝学组, 中华医学会肝病学分会重型肝病与人工肝学组. 肝衰竭诊治指南 (2018 年版). 临床肝胆病杂志,2019, 35(1): 38-44.
8. European Association for the Study of the Liver. EASL 2017 Clinical Practice Guidelines on the management of hepatitis B virus infection. J Hepatol. 2017 Aug;67(2):370-398.
9. Huang KW, Tam KW, Luo JC, et al.Efficacy and Safety of Lamivudine Versus Entecavir for Treating Chronic Hepatitis B Virus-related Acute Exacerbation and Acute-on-Chronic Liver Failure: A Systematic Review and Meta-Analysis.J Clin Gastroenterol. 2017 Jul;51(6):539-547.
10. Shim JH,Lee HC.Kim KM.et al.Efficacy of entecavir in treatment-naive patients with hepatitis B virus-related decompensate cirrhosis. J Hepatol. 2010, 52: 176-182.
11. Wan YM, Li YH, Xu ZY, et al. Tenofovir Versus Entecavir for the Treatment of Acute-on-Chronic Liver Failure due to Reactivation of Chronic Hepatitis B With Genotypes B and C.J Clin Gastroenterol. 2019 Apr;53(4):e171-e177.
12. Chan HL, Lim YS, Seto WK, et al. Three Year Efficacy and Safety of Tenofovir Alafenamide (TAF) Compared to Tenofovir Disoproxil Fumarate (TDF) in Hbeag-Negative and Hbeag-Positive Patients with Chronic Hepatitis B. AASLD2018 Poster 381.
13. 富马酸丙酚替诺福韦片(韦立得)产品说明书. 2018 年版.
14. FDA. Prescribing information: VIREAD® (tenofovir disoproxil fumarate). https://www.accessdata.fda.gov/drugsatfda_docs/label/2016/208464s000lbl.pdf
15. Gilead Sciences. Prescribing information: VEMLIDY® (tenofovir alafenamide). https://www.gilead.com/-/media/files/pdfs/medicines/liver-disease/vemlidy/vemlidy_pi.pdf

