谈到输血相关感染,人们首先想到的是肝炎、艾滋病等传染病。实际上,输血相关感染包括了输血传播的感染和输血的感染风险两部分。
输血传播的感染
自从 19 世纪 40 年代首例输血相关肝炎报道开始,人们便认识到输血会导致其携带病原体的传播。19 世纪 80 年代,艾滋病的蔓延给全球带来恐慌,输血不再仅仅被认为是一种救命的措施,同时也是致命性的。为此,世界各国积极采取了应对措施,主要包括对献血人群的规范、对捐献血液的传染源筛查和对血液进行加工灭活病原体。
1. 规范献血人群,修订献血政策
中国、丹麦、挪威、德国等国家终身禁止男同人群献血。我国 2012 年修订的《献血者健康检查要求》指出,易感染经血传播疾病的高危人群,如有吸毒史、男男性行为和多个性伴侣者等禁止献血。美国食品和药物管理局(FDA)在 2015 年 12 月修改原禁止男同人群献血政策为:一年内发生过男男性行为者禁止献血,这与包括法国、瑞典、爱尔兰在内的部分欧洲国家献血政策相同。
2. 筛查传染源
目前我国对捐献血液进行的传染源筛查主要包括:HBV、HCV、HIV、HTLV、梅毒等。然而,近期感染、仍处于感染窗口期的患者为筛查带来了很大的困难。核酸检测法(NAT)的应用大大提高了病原检出率,降低了输血感染率,但仍存在筛查病原不全面以及对新发传染病原筛查的局限。为此,一些国家采取了回顾计划(look-back scheme),即对接受了不充分筛查血液的受血者,以及输血后发现存在被感染可能的受血者和对应的献血者,进行长时间随访、检测和治疗,并在血库中移除所献血液及血液成分。
3. 对捐献血液进行加工,灭活病原体
白细胞去除法,降低寄居在白细胞内的病原体负荷,例如:巨细胞病毒,人类 T 淋巴细胞病毒,朊病毒(可能);
溶解-洗涤法,灭活血浆中的包膜病毒;
应用交联剂、烷化剂法破坏血液成分中的病原核酸;
新型灭活血细胞病原体方法:INTERCEPT 技术:合成能穿透细胞膜和核膜的补骨脂素 S-59,在 A 波紫外线照射下使之与病原体 DNA 或 RNA 的嘧啶环结合并破坏;MIRASOL 技术:利用核黄素的光敏作用破坏核酸;THERAFLEX UV 技术:应用窄带宽 C 波紫外线照射促进嘧啶二聚体形成,破坏核酸。
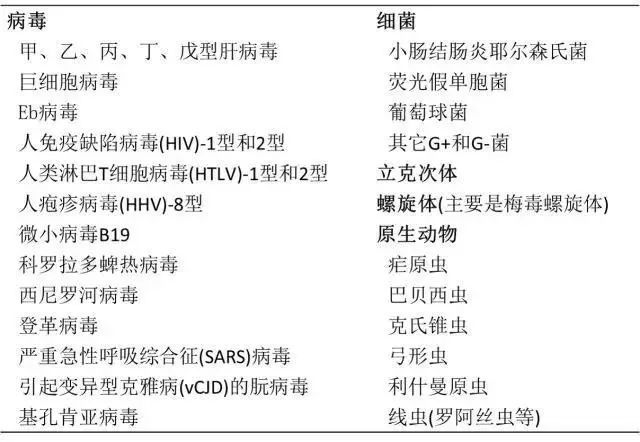
表 1 经输血传播的主要病原体
理论上,那些存在于献血者血液且未造成献血者任何临床感染症状,在血液加工和储存过程中仍能存活的病原体,将对输血安全造成威胁。2009 年,美国血库协会(American Association of Blood Banks,AABB)发现了 68 种潜在血液传播病原体,其中最重要的三个为:引起变异型克雅病(vCJD)的朊病毒,登革病毒和巴贝西虫。
该列表仍在不断扩大,至 2014 年,又新增了 6 种病原体(包括导致中东呼吸综合征的冠状病毒等)。病原灭活仍为重要的应对策略,对受血者持续的监测、风险评估和及时干预也尤为重要。FDA 在 2010 年对新发输血传播传染病威胁进行讨论发现,新发传染病多为动物源性,这可能与人类和野生动物接触增加,以及野生动物栖息地的变化有关。
目前,有效的应对措施已将常见输血传播的病毒感染发生率降到极低,据一项 1997 年至 2013 年的血库统计数据报道,输血传播 HCV 感染率已由 1.67 下降至 0.01(例/106 单位),输血传播 HBV 感染率已由 0.34 下降至 0.09(例/106 单位),输血传播 HIV 感染率已由 0.1 下降至 0.04(例/106 单位)。然而,由于临床上输血的很大一部分人群为恶性血液病肿瘤患者,他们或存在粒细胞缺乏症,或合并其他机会性感染,在入院期间往往经验性或治疗性使用抗生素,因此输血传播的细菌感染往往被掩盖,或被认为是输血反应。
输血传播的细菌感染
1. 输血传播细菌感染和死亡风险
根据法国国家血液警戒系统 2000~2008 年数据,输血传播细菌感染发生率为:2.45 例/106 单位血细胞,24.7 例/106 单位血小板和 0.39 例/106 单位红细胞。其中,输血小板相关死亡率最高,为 5.14 例/106 输血单位。
输血相关败血症是第二常见的输血相关死亡原因,死亡率大约在 1 例/6*106 单位。1995 年 10 月至 2004 年 9 月,FDA 报道的输血相关败血症死亡率为 13%(85/665),其中大部分(68%,58/85)为 G-菌感染。
2009 至 2011 年,FDA 报道输血相关年死亡例数分别为 44 例,40 例和 39 例,其中分别有 5 例(11%),2 例(5%)和 4 例(13%)被证实为微生物感染,其中 2010 年和 2011 年的 6 例感染病原为巴贝西虫、金黄色葡萄球菌、大肠杆菌、摩氏摩根菌、肺炎克雷伯菌。
2. 输血传播细菌感染来源
献血者的血液
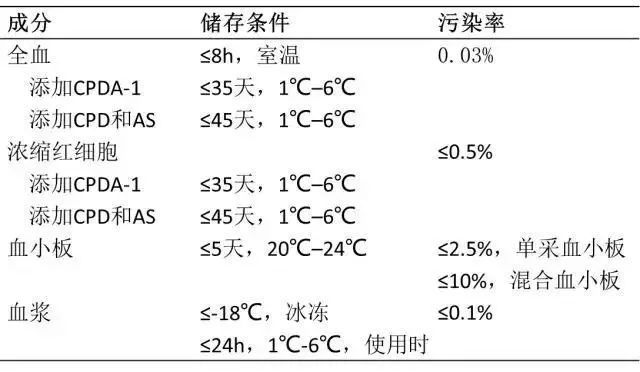
献血者有无症状性、低水平或一过性菌血症,而血液成分储存和加工条件又满足了微生物生长的需要。下面就不同血液成分及其储存条件和常见感染病原体做一小结。
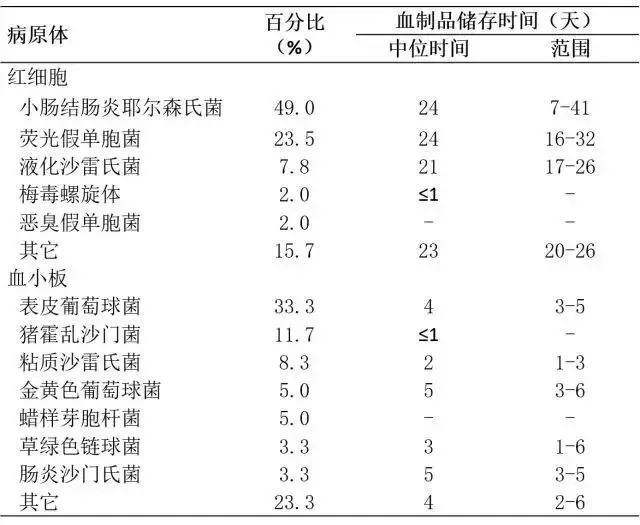
环境和皮肤
环境是皮肤污染的主要来源。采血时带入的皮肤表面病原体,如表皮葡萄球菌,一直被认为是血液污染的来源之一。有研究提示,将采血最初的 10~40 ml 移除,不输入采血容器(可用做病毒检测等),可降低 95%~98% 皮肤表面细菌污染率。另一项前瞻性临床研究表明,移除采血最初的 10 ml,总体细菌污染率由 0.35% 下降至 0.21%(P = 0.05),葡萄球菌污染率由 0.14% 下降至 0.03%(P<0.02)。
容器/注射用品
丹麦和瑞典曾先后报道了两例由集血袋污染引起的沙雷氏菌菌血症,随后丹麦对 1515 个集血袋进行了回顾性沙雷氏菌污染调查,在 11(0.73%)个集血袋中检测到了沙雷氏菌,对应输血患者中有 3 名出现了菌血症,这 3 名患者的临床分离株、集血袋中的菌株和植物来源的沙雷氏菌株有相同的核糖体型。
3. 干预措施

输血的感染风险
一方面,同种异体血液具有免疫活性,输血后可发生各种类型的免疫和超敏反应,都涉及免疫系统结构域的激活;另一方面,同种异体血液也有抑制免疫系统作用。输血相关免疫调节(transfusion-related immunomodulation,TRIM)作用机制不明,但临床观察发现和肿瘤复发和术后感染相关,推测原因可能与异体血液中的白细胞、残余的等离子体和其他存储介质及生物活性物质有关。
另一增加输血相关感染风险的因子是血液中的铁离子,每 300 ml 全血中约有 200 mg 血红素铁,与可溶性铁不同,血红素结合铁可供微生物生长。因此,即使所输血液本身并不携带感染病原体,输血也可能使机体对其他病原体更加易感,如增加院内感染几率。有荟萃分析、近期多个观察性分析和临床实验都证实了这一观点。
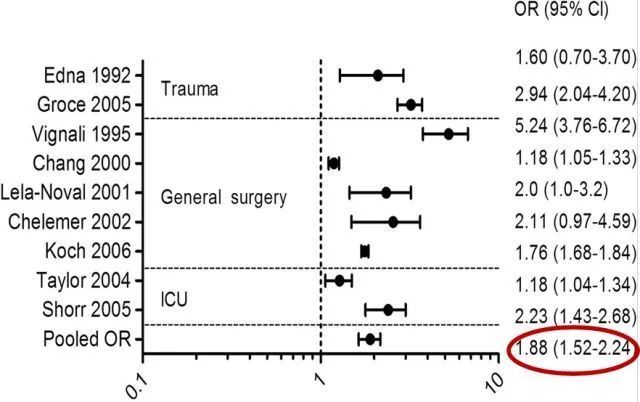
一项纳入了 45 篇(272,596 例)临床研究的荟萃分析旨在评估输注红细胞的利弊,得到结论红细胞输注为院内感染的独立危险因素(OR 1.8;95%CI 1.5-2.2)。
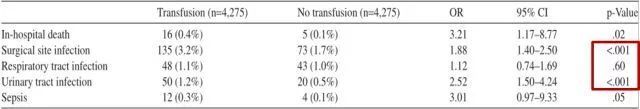
Kato S 等纳入了 84,000 例腰椎手术患者,倾向匹配分析后发现输血病人更易发生手术部位感染(OR 1.9;95%CI 1.4-2.5)或尿路感染(OR 2.5;95%CI 1.5-4.2)。
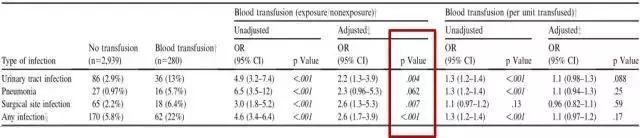
这与 Janssen SJ 等人的研究结果一致,他们同样纳入腰椎手术人群(3721 例),应用多因素回归分析得出输血与术后感染独立相关(OR 2.6;95%CI 1.7-3.9),与肺部感染无关,同时也未发现输血量与感染有关。
另外,Friedman R 等在关节置换术(髋关节或膝关节成型术)人群中的研究(12,000 例)提示输血患者术后感染率为 9.9%,显著高于未输血患者的 7.9%(P = 0.003),且输血患者更易发生肺部感染(P = 0.002),和伤口感染(P = 0.046)。在心脏手术人群中,每多输一个单位的红细胞可增加术后平均 29% 的感染风险。
小结
1. 输血相关感染包括输血传播的感染和输血的感染风险两部分;
2. 输血传播的感染是同种异体输血最早发现的输血风险之一。目前,高效的筛查手段已将人们所熟知的经输血传播感染风险降到很低;
3. 控制和预防输血传播感染的策略集中在:对高危献血者的筛选,应用多种方法检测血液中存在的潜在病原体,血液中的病原体灭活;
4. 理论上存在的输血传播新发感染病原体仍是潜在的威胁,如朊病毒,登革热病毒,巴贝西虫和导致中东呼吸综合征的冠状病毒等;
5. 输血传播的细菌感染仍较常见,其中血小板最易被污染,主要污染来源为血液、环境、皮肤和容器/注射用品;
6. 医院感染已经成为同种异体输血最常见的感染性风险。即使所输血液本身不携带感染病原体,输血也会使得机体更易获得新的感染。大量观察性研究以及输血相关临床试验,明确了输血和感染风险之间的联系;
7. 合理、基于循证地使用血制品和应用合理的患者血液管理策略,可降低输血相关感染风险。
编辑|安佳蔷
扫描下方二维码关注「丁香智汇」,阅读更多精彩文章!